Zum biologischen Schicksal von Chemikalien
Die Wirkweise von Wirkstoffen ist in verschiedenen Organismen unterschiedlich
Unser gegenwärtiges Leben ist unter anderem auch von naturfremden Stoffen gekennzeichnet, mit denen sich jeder Organismus, auch der des Menschen, auseinandersetzen muss. Chemikalien wurden zu einem Bestandteil der Umwelt und erreichen uns Menschen über Lebensmittel, Kosmetik- und Hygieneprodukte, sowie im produzierenden und verarbeitenden Gewerbe. Auch durch Medikamente werden sie in den Körper geschleust. Ähnlich wie Naturstoffe werden auch jene Xenobiotika verdaut. Das heißt, auch Xenobiotika unterliegen in den Zellen der Organe einem Stoffwechsel. Für die Verdauung der körperfremden, molekularen Substanzen bilden sich, vorwiegend in den Leberzellen, bestimmte Enzyme, die den Fortbestand dieser Moleküle verhindern.
Die Zellen des Immunsystems erkennen diese Xenobiotika nicht, zumindest nicht im Sinne der Abwehr von Mikroorganismen. Die Immunzellen erkennen „nur“ körperfremde Eiweißstoffe, die beispielsweise alle Bakterien mit sich tragen. Jedoch können auch Xenobiotika körpereigene Eiweißstoffe verfremden, sodass diese von den Immunzellen als fremd erkannt und bekämpft werden; wie es etwa bei Kontaktallergenen der Fall ist.
Wenn nun alles glatt ablaufen würde, das heißt durch den Stoffwechselprozess nichts entsteht, das irgendeine Körperzelle attackiert, oder der eingedrungene Stoff selbst nichts anrichtet, gäbe es viele, insbesondere medizinische Fachgebiete nicht. Eines dieser Fachgebiete wäre die Toxikologie, denn etliche Stoffe oder Stoffwechselprodukte (Abbauprodukte, Metaboliten) dieser Xenobiotika attackieren Zellproteine, Zellmembranen oder die Gene, die (organspezifisch) für die Zellfunktionen nötig sind.
Treibt einen die Neugierde für dieses Thema über die Lehrbücher der Toxikologie hinaus, stößt man unwillkürlich auf zwei Fachzeitschriften, die in ihrem Titel und Untertitel genau das ausdrücken, was man wissen will: Die eine, „Xenobiotica – the fate of foreign compounds in biological systems“, betrachtet das Thema von der toxikologischen Seite und die andere, „Drug Metabolism and Disposition – the biological fate of chemicals“, von der pharmakologischen Seite. Beiden gemeinsam ist der Untertitel, frei übersetzt: „Zum biologischen Schicksal körperfremder Stoffe“.
Biotransformation
Das Gebiet der Toxikologie ist umfangreich und soll hier nur für den Bereich des Stoffwechsels auf zellulärer Ebene skizziert werden. Den normalen Weg, den ein xenobiotischer Stoff durch die Zelle geht, beginnt mit dem Durchdringen der äußeren Zellmembran. Er unterliegt dann der Wechselwirkung mit den zelleigenen Eiweißstoffen (Proteine) und verlässt dann wieder, als veränderte Substanz, die Zelle. Die Zufuhr des Stoffes und die Abfuhr dessen Metaboliten erfolgt über den Bereich zwischen den Zellen (interzellulären Raum) und des Blutstromes.
Der Transport durch Zellmembranen spielt eine wichtige Rolle, da die Biotransformation in verschiedenen Zellteilen erfolgt. Dieser Punkt ist aber Gegenstand einer relativ jungen Wissenschaft und daher weit weniger im Detail erforscht als die Biotransformation.
Unter der Biotransformation versteht man im Allgemeinen die Veränderung eines Stoffes zu einem mit dem Urin ausscheidungsfähigen und daher wasserlöslichen Abbauprodukt. Diese unter der Bezeichnung Metabolismus 1) bekannte Überführung erfolgt in zwei Phasen. Die Phase I entspricht einer Oxidation des Stoffes, das heißt, das eingedrungene Molekül wird vermittels Sauerstoff an bestimmten Stellen oxidiert. Chemisch betrachtet entstehen beispielsweise Epoxide, die letztlich in verschiedenartige hydroxidische Verbindungen (also Sauerstoff-Wasserstoff-Gruppen am Molekül) enden.
|
Durch die Oxidationsphase der Metabolisierung sind die Stoffe in der Art präpariert, dass die Metabolisierung in die Phase II, der so genannten Konjugation, übergehen kann. Dabei werden „biologische“ Molekülteile, vermittels so genannter Transferasen, an die oxidierten Moleküle angelagert, sodass letztlich ein Metabolit entsteht, der „gefahrlos“ aus der Zelle, und weiter aus dem Organismus entfernt werden kann.
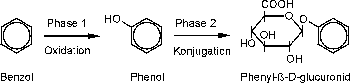
Beispielsweise wird Benzol, wie in Abbildung 1 illustriert, in der ersten Phase zu Phenol oxidiert und in der zweiten Phase entsteht ein gut wasserlösliches Konjugat durch Glucuronosyltransferase: das Phenyl-ß-D-glucuronid. Über diesen Weg kann also Benzol ausgeschieden und damit entgiftet werden. Andererseits entstehen in der oxidativen Phase des Benzols, die wesentlich komplexer ist als in Abbildung 1 gezeigt, auch reaktive Metaboliten, die unter anderem für die Knochenmarkstoxizität verantwortlich sind.
Einige Metaboliten sind also nach wie vor eine Gefahr. Zum Beispiel dann, wenn sie nicht, oder nicht schnell genug in die zweite Phase der Metabolisierung gelangen oder nicht aus der Zelle heraustreten können, weil bestimmte Trägerproteine (etwa das P-Glycoprotein) den Austritt verhindern.
Details der Phase I
Die Metaboliten der Phase I stellen eine potentielle Gefahr für die inneren Bestandteile der Zelle dar, da sie für den Transport aus der Zelle nicht gut geeignet sind. Für etliche typische Umweltgifte sind die Mechanismen dieser Phase gut aufgeklärt.
Im Gegensatz zur Konjugation, der zweiten metabolischen Phase, die in der Zellflüssigkeit (Zytosol) stattfindet, läuft die Oxidation der ersten metabolischen Phase im endoplasmatischen Retikulum 2) ab. In diesem Teil der Zelle befinden, genauer gesagt bilden sich die Metabolisierungsenzyme, die als Cytochrom P450 in die Literatur eingegangen sind 3) . Die Cytochrom P450-Enzyme, kurz CYP-Enzyme, sind gegenwärtig in 74 Genfamilien (für Wirbeltiere) eingeteilt, von denen 14 Familien mit mehreren Subfamilien in Säugetieren vertreten sind. Mit der Anwesenheit eines Fremdstoffes in der Zelle werden bestimmte Typen einer oder mehrerer CYP-Subfamilien ausgebildet (exprimiert) oder deren Ausbildung verhindert 4) .
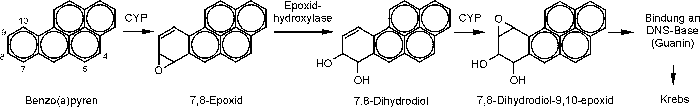
Für viele Umweltschadstoffe und Arzneimittel sind die ausgebildeten CYP-Enzyme bekannt. Das heißt, jedes der verschieden geprägten Enzyme „erkennt“ sein vorbestimmtes Fragment am fremden Molekül. Für polyzyklische aromatische Kohlenwasserstoffe (PAK), das sind Umweltschadstoffe wie Benzo(a)pyren, sind unter anderem einige Enzyme der Familie 1 (CYP1A1, CYP1A2) und Familie 2 (CYP2B1, CYP2C9) für deren Metabolisierung verantwortlich. Für Glycocortikoide (Cortison) spielen beispielsweise CYP3A-Enzyme aus der Familie 3 und dessen Subfamilie A, eine wesentliche Rolle bei der Umsetzung dieser Substanz.
Mit der Entdeckung der CYP's und deren Rolle bei der Metabolisierung von Fremdstoffen in Organismen war und ist es möglich, den Mechanismus zur Auslösung von Erkrankungen aufzuklären und sogar vorauszusagen.